- Elektromagnetische Felder
- Gefahrenschwerpunkt Frachtcontainer
- Innenraumarbeitsplätze
- Kühlschmierstoffe
- Praxishilfen: Ergonomie
- Praxishilfen: Gefahrstoffe
- Praxishilfen: Lärm
- Praxishilfen: Maschinenschutz
- Praxishilfen: Persönliche Schutzausrüstungen
- Praxishilfen: Vibration
- Produktsicherheit
- Tätigkeiten mit krebserzeugenden Gefahrstoffen
Kohlenwasserstoffe
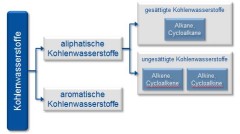
Unter Kohlenwasserstoffen fasst man organische Verbindungen zusammen, die aus den Elementen Kohlenstoff und Wasserstoff bestehen. Das Element Kohlenstoff besitzt die Fähigkeit zur Bildung von Kohlenstoff-Kohlenstoff-Bindungen verschiedenster Art. Dadurch entstehen unzählige Verbindungen. Basierend auf ihrer chemischen Reaktivität teilt man sie in verschiedene Stoffklassen ein (siehe Bild).
Aliphatische Kohlenwasserstoffe unterscheidet man in gesättigte und ungesättigte Verbindungen.
Gesättigte Kohlenwasserstoffe (Alkane, früher auch Paraffine genannt) enthalten lediglich Kohlenstoff-Kohlenstoff-Einfachbindungen in ihrem Gerüst. Ist das Kohlenstoffgerüst ringförmig angeordnet, spricht man von Cycloalkanen (früher auch Naphthene genannt). Alkane sind aufgrund ihres gesättigten Charakters (keine Doppelbindungen) und durch das Fehlen von funktionellen Gruppen reaktionsträge.
Ungesättigte Kohlenwasserstoffe unterteilt man in Verbindungen, die eine oder mehrere Kohlenstoff-Kohlenstoff-Doppelbindungen enthalten (Alkene), und solche, die eine oder mehrere Kohlenstoff-Kohlenstoff-Dreifachbindungen enthalten (Alkine). Auch hier treten wieder kettenförmige und ringförmige (Cyclo-)Molekülstrukturen auf. Ungesättigte Kohlenwasserstoffe reagieren relativ leicht. Die bevorzugte Reaktion ist eine Addition an die Mehrfachbindung.
Aliphatische und cycloaliphatische Kohlenwasserstoffe sind überwiegend farblose Substanzen. Die flüssigen Verbindungen riechen benzin- bzw. petroleumartig und sind aufgrund ihres unpolaren Charakters mit stark polaren Lösemitteln (zum Beispiel Wasser) nicht mischbar.
Neben den aliphatischen Kohlenwasserstoffen gibt es die große Gruppe der aromatischen Kohlenwasserstoffe. Dabei handelt es sich um cyclische Moleküle, die über ein konjugiertes Doppelbindungssystem verfügen. Aromatische Kohlenwasserstoffe sind sehr stabile Verbindungen. Aufgrund ihres Bindungssystems sind sie jedoch Substitutionsreaktionen leicht zugänglich.
Kohlenwasserstoffe dienen als Brennstoffe, Motorkraftstoffe, Lösemittel, Schmierstoffe und als Ersatz für Treibgase. Sie werden aus Erdgas, Erdöl oder Kohle gewonnen und durch verschiedene Verfahren der Petrochemie (Destillation, Cracken, Reformieren usw.) veredelt.